Respecto al artículo Factores de riesgo de carcinoma hepatocelular en pacientes con infección crónica por virus de hepatitis C en tratamiento con interferón pegilado-ribavirina
About the paper Risk factors of hepatocellular carcinoma in patients with chronic hepatitis C virus infection receiving pegylated interferon ribavirin treatment.
Med Int Méx 2022; 38 (2): 476-478. https://doi.org/10.24245/mim.v38i2.6966
Madelaine Margaritté Navarro-Yparraguirre,1 Andrés Omar Arias-Revilla,1 Juan Carlos Ezequiel Roque-Quezada2
1 Estudiante de Medicina Humana
2 Médico cirujano. Magister en Medicina.
Facultad de Medicina Humana, Universidad Ricardo Palma, Lima, Perú.
Sr. Editor
Hemos leído con bastante interés el artículo “Factores de riesgo de carcinoma hepatocelular en pacientes con infección crónica por virus de hepatitis C en tratamiento con interferón pegilado-ribavirina” de Marco Tobar-Marcillo y colaboradores,1 donde se evalúa a pacientes en tratamiento con interferón pegilado (INF-pg)-ribavirina (RBV) que tuvieron carcinoma hepatocelular y se comparan con pacientes que recibían el mismo tratamiento que no lo padecieron. En este contexto, quisiéramos realizar algunos comentarios sobre los criterios de valoración durante el tratamiento mencionado en ese artículo.
Según estadísticas recientes, la infección crónica causada por el virus de hepatitis C es una enfermedad que afecta a más de 180 millones de personas mundialmente,1,2 es la principal causante de cirrosis, hepatocarcinoma y de trasplante hepático. Alrededor del 30% de los casos de cirrosis hepática y cerca del 15% de los casos de carcinoma hepatocelular son causados por el virus de la hepatitis C en todo el mundo,3 generando así una carga social y económica.
Desde el decenio de 1990 hasta ahora, se ha producido un aumento espectacular en la capacidad de eliminar el virus de la hepatitis C y esto se debe a los tratamientos con inhibidores directos del virus en niveles de la proteasa o los antivirales de acción directa contra el virus C con eficacia de eliminación del 90 al 100% cuando inicialmente era solo del 7 al 11%.4 Figura 1
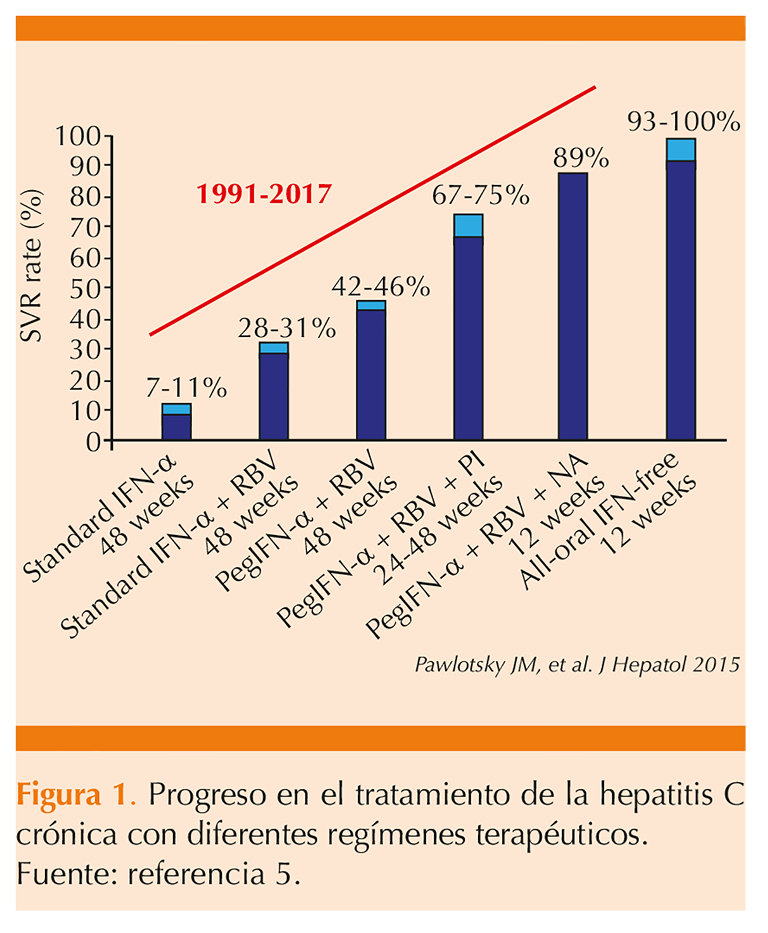
Desde inicios de 1991, se empezó con el interferón. Pero, a partir de 2014 empezaron los antivirales de acción directa, como el daciatasvir, simeprevir y sotosbuvir, permitiendo aumento del 50% en la eliminación del VHC. Sin embargo, en 2016 y 2017 aparieron Epclusa, Vosevi y Maviret, que eliminan casi en el 98 al 100% el virus de la hepatitis C.4
El uso de estos antivirales de acción directa en los últimos años ha tenido un efecto tremendo en la disminución de los pacientes en lista de espera para trasplantes hepáticos.5 Esto se refleja en que la indicación de trasplante hepático por VHC ha disminuido notablemente desde 2014 en Estados Unidos y actualmente la indicación de trasplante por enfermedad alcohólica y NASH se volvieron las principales.6 Figura 2
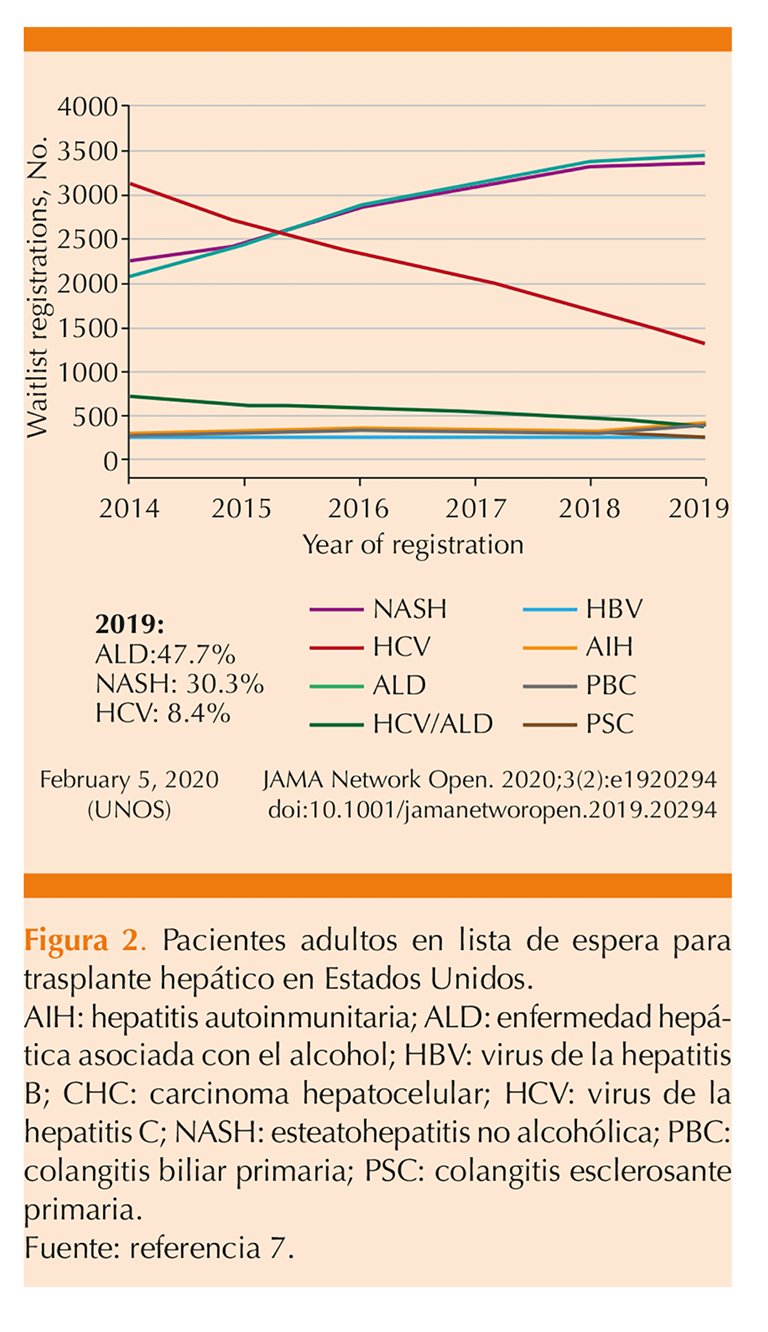
Entonces, haber disminuido la indicación por trasplante por VHC gracias a los antivirales de acción directa permite un espacio para otras indicaciones. En 2035 se va a ahorrar en Estados Unidos 7320 hígados que hubieran sido destinados para enfermos con cirrosis por VHC y serán destinados para pacientes con cirrosis por virus no C.7
Por último, es de mencionar que gracias a los nuevos antivirales de acción directa, se acepta mayor cantidad de donantes con VHC positivo porque, con el nuevo tratamiento, se podrá eliminar el virus.
REFERENCIAS
1. Tobar M, López J. Factores de riesgo de carcinoma hepatocelular en pacientes con infección crónica por virus de hepatitis C en tratamiento con interferón pegilado-ribavirina. Med Interna México 2021; 37 (4): 469-74. https://doi.org/10.24245/mim.v37i4.3868
2. Alter MJ. Epidemiology of hepatitis C virus infection. World J Gastroenterol 2007; 13 (17): 2436-41. doi: 10.3748/wjg.v13.i17.2436.
3. Mohd Hanafiah K, Groeger J, Flaxman AD, Wiersma ST. Global epidemiology of hepatitis C virus infection: new estimates of age-specific antibody to HCV seroprevalence. Hepatol 2013; 57 (4): 1333-42.
4. Perz JF, Armstrong GL, Farrington LA, Hutin YJF, Bell BP. The contributions of hepatitis B virus and hepatitis C virus infections to cirrhosis and primary liver cancer worldwide. J Hepatol 2006; 45 (4): 529-38. doi: 10.1016/j.jhep.2006.05.013.
5. Pawlotsky J-M, Feld JJ, Zeuzem S, Hoofnagle JH. From non-A, non-B hepatitis to hepatitis C virus cure. J Hepatol 2015; 62 (1 Suppl): S87-99. https://doi.org/10.1016/j.jhep.2015.02.006.
6. Flemming JA, Kim WR, Brosgart CL, Terrault NA. Reduction in liver transplant wait-listing in the era of direct-acting antiviral therapy. Hepatol 2017; 65 (3): 804-12. doi: 10.1002/hep.28923.
7. Wong RJ, Singal AK. Trends in liver disease etiology among adults awaiting liver transplantation in the United States, 2014-2019. JAMA Netw Open 2020; 3 (2): e1920294. doi:10.1001/jamanetworkopen.2019.20294
Recibido: 12 de octubre 2021
Aceptado: 4 de noviembre 2021
Este artículo debe citarse como: Navarro-Yparraguirre MM, Arias-Revilla AO, Roque-Quezada JCE. Respecto al artículo Factores de riesgo de carcinoma hepatocelular en pacientes con infección crónica por virus de hepatitis C en tratamiento con interferón pegilado-ribavirina. Med Int Méx 2022; 38 (2): 476-478.
Sin comentarios